Trasformazione di energia chimica in energia elettrica. Potenziale d'elettrodo. Pila elettrica
Un metallo (Me) che viene immerso in una soluzione di un suo sale (contenente quindi suoi ioni positivi) manifesta una sua propria tendenza a passare in soluzione trasformandosi esso stesso in ione positivo, Men+:
che è dato dalla somma delle semireazioni di ossidazione e di riduzione prima descritte. Le soluzioni nelle due semicelle possono essere collegate da un ponte salino o separate da un setto poroso, permeabile agli ioni (che svolge la stessa funzione). Il ponte salino o il setto poroso hanno cioè lo scopo di chiudere il circuito, consentendo l'elettroneutralità del sistema. Infatti la diffusione di ioni negativi dal ponte salino nello scoparto anodico compensa le cariche positive dello zinco che passa in soluzione e la diffusione di ioni positivi nello scomparto catodico compensa l'eccesso di ioni negativi che si avrebbe dopo la deposizione degli ioni Cu2+ al catodo.
Media correlati
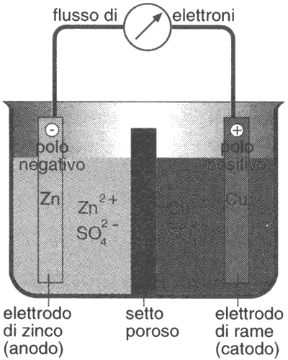
Figura 15.1 Schema di pila Daniell nella versione con setto poroso anziché ponte salino (si veda il testo). In essa la corrente è generata da un flusso di elettroni trasferiti dall'elettrodo di Zn all'elettrodo di Cu.


