La sintesi proteica
Si definisce sintesi proteica il processo con cui una sequenza di nucleotidi viene convertita nella successione di amminoacidi formanti una proteina. Alla sintesi proteica prendono parte attiva l'm-RNA, il t-RNA e l'r-RNA.
L'm-RNA copia l'informazione contenuta nel DNA e la trasporta dal nucleo al citoplasma (questo stadio è detto trascrizione); il t-RNA e l'r-RNA traducono il messaggio scritto sull'm-RNA in una sequenza di amminoacidi (questo stadio è detto traduzione). Durante la sintesi proteica perciò, l'informazione genetica passa dal DNA all'RNA e dall'RNA alle proteine. È questo il dogma centrale della biologia.
 La trascrizione
La trascrizione
La trascrizione è lo stadio della sintesi proteica in cui le informazioni sono trasferite dal DNA all'RNA, secondo le regole dell'appaiamento delle basi complementari.
Come nella replicazione , è necessario che le basi azotate sporgano dalla doppia elica del DNA. Perciò il tratto di DNA che deve essere trascritto viene aperto in un punto ben preciso, caratterizzato dalla tripletta AUG di "inizio lettura". Un enzima, l'RNA-polimerasi, si lega a uno dei due filamenti di DNA che serve da "stampo", e procede dall'estremità 3' all'estremità 5' legando i ribonucleotidi complementari presenti nel nucleo. Si forma in questo modo l'm-RNA.
Quando l'RNA-polimerasi giunge alla tripletta di "fine lettura", l'm-RNA si separa dalla catena di DNA, passa per i pori della membrana nucleare ed entra nel citoplasma, dove si lega ai ribosomi. Il DNA "modello" si riavvolge a formare la doppia elica, oppure si lega a una nuova molecola di RNA-polimerasi per sintetizzare un nuovo filamento di m-RNA.
La traduzione è lo stadio della sintesi proteica in cui le istruzioni portate dall'm-RNA vengono tradotte nella sequenza corretta di amminoacidi per formare una proteina.
La traduzione (v. fig. 5.6) ha luogo nel ribosoma (formato da r-RNA e proteine), composto da due subunità: quella piccola contiene un sito di legame per l'm-RNA; quella grande ha due siti di legame per due molecole di t-RNA e un sito che catalizza la formazione del legame peptidico tra due amminoacidi adiacenti.
Ogni molecola di t-RNA è specifica per un unico amminoacido ed è in grado di riconoscere sia l'amminoacido che deve trasportare, sia il codone complementare di m-RNA associato al ribosoma.
La traduzione ha inizio quando due codoni del filamento di m-RNA si legano alla subunità piccola di un ribosoma. Il primo codone è la tripletta di "inizio lettura" AUG, alla quale corrisponde l'amminoacido metionina; il secondo codifica il primo vero amminoacido della proteina. I due t-RNA, che hanno rispettivamente l'anticodone di inizio e l'anticodone complementare al secondo codone, si legano alla subunità grande e si forma un legame peptidico (cioè il legame tra amminoacidi che forma le proteine) tra i due amminoacidi trasportati.
Il t-RNA di inizio si stacca dal ribosoma mentre il dipeptide (i due amminoacidi uniti dal legame peptidico) rimane legato al secondo t-RNA. Il ribosoma si sposta sopra un altro codone dell'm-RNA e una nuova molecola di t-RNA con il proprio amminoacido si dispone nel sito di legame vuoto del ribosoma. Si crea un nuovo legame peptidico e il tripeptide si salda all'ultimo t-RNA. Il processo di allungamento della catena polipeptidica prosegue in questo modo finché tutte le triplette sono state tradotte e viene raggiunto il codone di "fine lettura". La proteina completa si stacca dal ribosoma e specifici enzimi scindono il legame con la metionina.
Media correlati
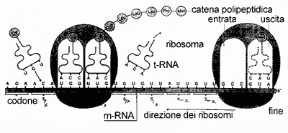
Figura 5.6 Il processo di traduzione.


